研究揭秘细菌膜中的抗菌肽活性
发表时间:2021-08-05
(AMPs)在天然免疫系统中被广泛研究,在对抗由多个耐药菌株引起的预感染性疾病方面很有潜力。与传统的抗菌肽相比,AMPs通过非特定的分子作用(静电、疏水、熵)易位,尽管最终的靶点也被定位在细胞溶质室中,但有3种不同的AMP/脂质相互作用模型被报道,包括跨膜感受孔的形成、胶束化或界面活性,这种模式可能导致表面吸附肽层(地毯)的形成或肽自身聚集。肽重组也被认为是加速脂滴,并最近被证实为对称的脂滴膜。
另一方面,结合受体的模式取决于脂质层的共同位置。也就是说,AMPS不能成为五孢子形式,也不能不考虑其靶膜的组成。重要的是,细菌膜上稳定的磷脂是磷脂酰甘油(PG),磷脂酰乙醇胺(PE)和心磷脂。
近期,在《Faraday Discuss》杂志上就发表了一篇相关的综述,名为“Antimicrobial peptide activity in asymmetric bacterial membrane mimics”。在该篇综述中,报道了由棕榈酰甲酰磷酸、棕榈酰乙酰胺和棕榈酰甲酰磷酸甘油酯组成的对称性膜与肽L18W-PGLA和Magainin2(MG2a)的相互作用,以及脂铁代谢水平F11-215的反应。
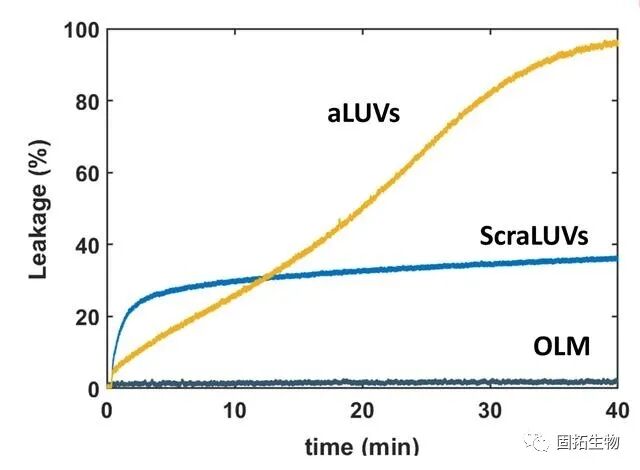
该项研究特别确定了肽诱导的脂滴流,以及膜分离FL18W-PGLA和LF11-215,18W-PGLa引起的气泡泄漏。L18W-PGLa 和 MG2a 通过膜易位的能力似乎与观察到的脂质触发器相关,L18W-PGLa 的发生速度最快。LF11-215 更高的结构灵活性反过来又允许该肽插入双层,而不会检测到膜不对称性的变化。因此,增加18W-PGLa膜的对称性和渗透性的脆弱性似乎是由组成层之间的张力差引起的,但不是因为增加了分区。
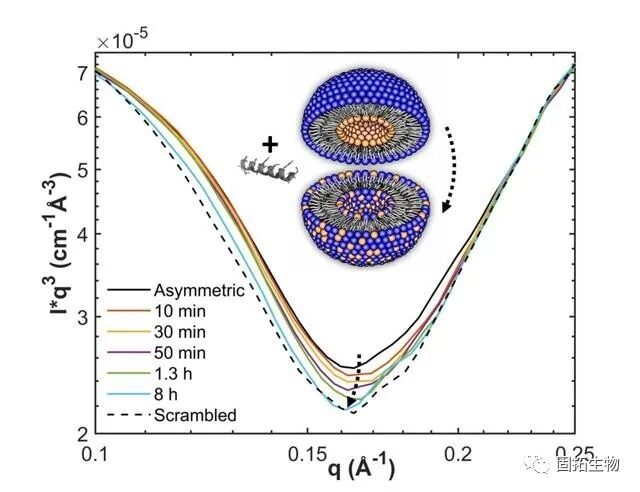
研究人员采用了对称的大型单腔静脉导管(ALUV),由棕榈酰甲酰磷酸酯乙醇胺(POPE)和棕榈酰甲酰磷酰甘油(POPG)组成,使用18W PGLa,以及Asmagainin2a(MG2a)和铁氧体去极化剂F11-215,特别是允许三种主要的表面EBoundNPE/PG膜,利用TrpEmission光谱法,通过对全角度中子散射(SANS)的测量,解决了液滴泄漏和肽分离的问题。
这项研究的结果揭示了肽浓度依赖于膜不对称性的缺失,而膜不对称性在18W PGLa中最为突出,遵循YMG2A。LF11-215尽管在ALUVS中的高分割性,但其内部引起的不可检测的脂质折叠。这表明FLF11-215的高结构-自然灵活性使肽能够在不对称的膜上转运,而不会对膜结构产生明显的影响。对于这些肽,L18W-PGLA和MG2A,lipidflip-Flop似乎与转移概率相耦合。与对称泡状物相比,18W PGLA存在时的渗透性增加不是由于增加了泡状物的分区,而是由于泡状物之间的内部横向应力平衡引起的。
膜的对称性使另一层的复杂性增加到一个临时的微生物肽活性。这里使用的DALUV可以看作是革兰氏阴性细菌胞外膜的一级模拟。而具有“正确”不对称性和成分的细胞质膜模拟是环糊精介导的脂质变化的某种适应性的先导,目前的研究得出了生理相关性的结论。
首先,根据先前的发现,包括细胞质细菌膜的心磷脂(对称)模拟物,反式双层脂质对称性使得双层由于膜小叶的不同长度而不易受损。然而,我们不能排除热膜实体(如蛋白质)有助于平衡这些差异。其次,我们的研究对仅在类脂和细菌中观察到的渗漏和抗微生物活性的观点进行了协调。当将细胞和膜组学的生物物理研究相结合时,对两者的深入理解似乎是一致的。
写到最后:
研究揭秘细菌膜中的抗菌肽活性?固拓生物科技有限公司为一家专业生产多肽合成、多肽定制的生产厂家,也有供应多肽原材料,选择固拓生物,你值得拥有,欢迎需要购买多肽的公司前来购买。